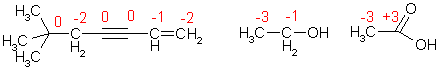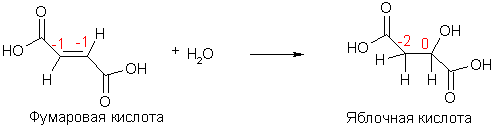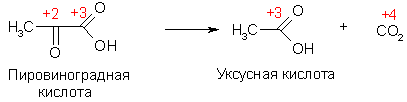Форму объемной восьмерки имеет орбиталь
Орбитальное квантовое число `l` показывает, сколько энергетических подуровней составляют данный уровень и характеризует форму орбиталей. Принимает значения от `0` до `(n-1)`.
При `n=3`, `l` принимает уже три значения: `0` `(s)`; `1` `(p)` и `2` `(d)`. Таким образом, на третьем уровне три подуровня. Орбитали `d`-подуровня имеют форму двух перекрещённых объёмных восьмёрок либо объёмной восьмерки с перемычкой (рис. 1).
При `n=4`, значений `l` уже четыре, следовательно, и подуровней на четвёртом уровне четыре. К перечисленным выше добавляется `3` `(f)`. Орбитали `f`-подуровня имеют более сложную, объёмную, форму.
Магнитное квантовое число `ml` определяет число орбиталей на каждом подуровне и характеризует их взаимное расположение.
Принимает значения `-l` до `+l`, включая `0`.
При `l=1`, `m_l` принимает три значения: `−1`; `0`; `+1`. Значит, орбиталей на данном подуровне (`p`-подуровне) три. Так как `p`-орбитали представляют из себя объёмные восьмёрки (то есть линейной структуры), располагаются они в пространстве по осям координат, перпендикулярно друг другу (`p_x`, `p_y`, `p_z`).
При `l=2`, `m_l` принимает уже пять значений: `−2`; `−1`; `0`; `+1`; `+2`. То есть на `d`-подуровне располагаются пять орбиталей. Это плоскостные структуры, в пространстве занимают пять положений.
Спиновое квантовое число `m_s` характеризует собственный момент количества движения электрона и принимает только два значения: `+1//2` и `-1//2`.
Всё вышесказанное можно обобщить в Таблице 2.
Таблица 2. Квантовые числа, атомные орбитали и число электронов на подуровнях (для `n
Форму объемной восьмерки имеет орбиталь
Главное квантовое число `n` определяет полную энергию электрона на энергетическом уровне и показывает, из скольких энергетических уровней состоит электронная оболочка атома. Принимает целочисленные положительные значения от `1` до `oo`. В периодической таблице Д. И. Менделеева `n` равно номеру периода.
Орбитальное квантовое число `l` показывает, сколько энергетических подуровней составляют данный уровень и характеризует форму орбиталей. Принимает значения от `0` до `(n – 1)`.
При `n=3`, `l` принимает уже три значения: `0(s)`; `1(p)` и `2(d)`. Таким образом, на третьем уровне три подуровня. Орбитали `d`-подуровня имеют форму двух перекрещенных объёмных восьмёрок либо объёмной восьмёрки с перемычкой (рис. 1).
При `n=4` значений `l` уже четыре, следовательно, и подуровней на четвёртом уровне четыре. К перечисленным выше добавляется `3(f)`. Орбитали `f`-подуровня имеют более сложную, объёмную, форму.
Магнитное квантовое число `ml` определяет число орбиталей на каждом подуровне и характеризует их взаимное расположение.
Принимает значения от `-l` до `+l`, включая `0`.
При `l=1`, `m_l` принимает три значения: `−1`; `0`; `+1`. Значит, орбиталей на данном подуровне (`p`-подуровне) три. Так как `p`-орбитали представляют из себя объёмные восьмёрки (то есть линейной структуры), располагаются они в пространстве по осям координат, перпендикулярно друг другу `(p_x,p_y,p_z)`.
При `l=2`, `m_l` принимает уже пять значений: `−2`; `−1`; `0`; `+1`; `+2`. То есть на `d`-подуровне располагаются пять орбиталей. Это плоскостные структуры, в пространстве занимают пять положений.
Ну и наконец, при `l=3`, то есть на `f`-подуровне, орбиталей становится семь, так как `m_l` принимает семь значений (от `−3` до `+3` через `0`). Орбитали являются более сложными объёмными структурами, и взаимное их расположение ещё более сложно.
`m_s` характеризует собственный момент количества движения электрона и принимает только два значения: `+1//2` и `-1//2`.
Электронная ёмкость подуровня (максимальное количество электронов на подуровне) может быть рассчитана по формуле `2(2l+1)`, а уровня — по формуле `2n^2`.
Всё вышесказанное можно обобщить в Таблице 2.
Таблица 2. Квантовые числа, атомные орбитали и число электронов на подуровнях (для `n
Форму объемной восьмерки имеет орбиталь
Атом состоит из положительно заряженного ядра и находящихся в его поле отрицательно заряженных электронов. Число электронов в атоме химического элемента равно положительному заряду ядра атома и порядковому номеру элемента в ПСХЭ.
Электроны в атомах могут располагаться на разных энергетических уровнях. Число энергетических уровней равно номеру периода, в котором находится элемент. Число электронов на внешнем (валентном) уровне атомов малых периодов равно номеру группы, в которой находится элемент.
Движущиеся электроны можно представить в виде электронного облака. Ближе к ядру оно относительно плотное. Область, в которой нахождение электрона наиболее вероятно, называют орбиталью.
Орбитали отличаются своей формой и размерами. Их обозначают латинскими буквами `s`, `p`, `d`, `f`. Каждая орбиталь характеризуется определённой энергией, и на ней не может быть более двух электронов. Орбитали `s`-типа имеет форму шара. Орбитали `p`-типа имеют форму объёмной восьмёрки (гантель); все три `p`-орбитали взаимно перпендикулярны и энергетически эквивалентны.
Атом углерода в органических соединениях находится в возбуждённом состоянии и его валентность равна четырём. Каждый неспаренный электрон атома углерода спаривается с неспаренным электроном атома водорода. Таким образом, атом углерода образует четыре ковалентные связи.
Теория гибридизации атомных орбиталей была разработана американским учёным Л. Полингом.
Предполагается, что при образовании химических связей орбитали всех валентных электронов атома углерода выравниваются и становятся одинаковыми. При этом все они принимают форму несимметричных, вытянутых в направлении к вершинам тетраэдра, объёмных восьмёрок, которые не имеют ничего общего как с `s`-, так и с `p`-орбиталями. Таким образом,
гибридизация представляет собой процесс выравнивания атомных орбиталей по форме и энергии.
Для атома углерода возможны три типа гибридизация (валентных состояния).
Чем больше область перекрывания (более тёмная часть на рисунке), тем большая электронная плотность сосредоточена в пространстве между ядрами и тем сильнее они «стягиваются». Поэтому `sigma`-связь отличается большей прочностью.
Таким образом, каждый атом углерода имеет по три гибридных электронных облака и по одному негибридному `p`-облаку. Гибридные электронные облака взаимно перекрываются и образуют между атомами углерода `sigma`-связь.
Двойная связь состоит из одной `sigma` и одной `pi` связей. `pi`-Связь образована перекрыванием двух негибридных `p`-орбиталей (по одной от каждого атома углерода), оси которых параллельны друг другу и расположены перпендикулярно плоскости `sigma`-связей.
Особый интерес представляют диеновые углеводороды, в которых содержатся две двойные связи, разделённые одной одинарной связью. Такие алкадиены называются сопряжёнными. Все четыре атомы углерода, стоящие рядом в сопряжённой системе, находятся в состоянии `sp^2`-гибридизации:
Все атомы углерода и водорода находятся в одной плоскости, а `p`-орбитали атомов углерода располагаются перпендикулярно этой плоскости. Боковое перекрывание `p`-орбиталей при образовании `pi`-связей происходит не только в положениях `1,2` и `3,4`, но и частично в положении `2,3`. Таким образом, `pi`-связи в сопряжённых диенах являются делокализованными и образуют единую `pi`-систему. Делокализацию `pi`-связей в сопряжённых диенах изображают структурной формулой:
Связь `»C»_2-«C»_3` носит кратный характер. Это подтверждается экспериментальным определением длин связей. Показано, что в бутадиене-`1,3` длина связи `»C»_2-«C»_3` `(0,146 «нм»)` несколько короче `sigma`-связей в алканах `(0,154 «нм»)`, но длиннее двойной связи `(0,133 «нм»)` в алкенах. А длина двойных связей в положениях `1` и `3` в бутадиене-`1,3` благодаря делокализации оказались несколько больше `(0,137 «нм»)`, чем в алкенах. Особенности образования `sigma`- и `pi`-связей и являются причиной своеобразия химических свойств сопряжённых диеновых углеводородов.
Другим соединением, в котором атом углерода находится в `sp^2`-гибридном состоянии, является бензол и его гомологи (ароматические соединения). Экспериментально установлено, что молекула бензола является плоской и все атомы углерода равнозначны, так же как и атомы водорода. Этот результат соответствует структурной формуле, предложенной Ф.А.Кекуле.
Было показано, что молекула бензола является правильным шестиугольником с одинаковыми расстояниями между ядрами атомов углерода `(0,140 «нм»)`, что противоречит формуле Ф.А. Кекуле. Равенство межъядерных расстояний говорит о том, что в бензоле нет одинарных и двойных связей, т. к. в этом случае одни расстояния между центрами атомов углерода были бы примерно равны `0,154 «нм»`, а другие – `0,134 «нм»`.
Все атомы углерода в молекуле бензола находятся в состоянии `sp^2`-гибридизации. При этом гибридные электронные орбитали каждого атомы углерода образуют в плоскости кольца две `sigma`-связи с соседними атомами углерода и одну `sigma`-связь с атомом водорода, следовательно, углы между этими тремя связями равны `120^@`.
Каждая орбиталь взаимодействует путём бокового перекрывания с орбиталями обоих соседних с ним атомов углерода. Поэтому в молекуле образуется не три отдельные `pi`-связи, а единая `pi`-электронная система из шести `p`-электронов, общая для всех атомов углерода. Такое равномерное распределение электронной плотности приводит к усреднению длин связей между атомами углерода.
`sp`-Гибридизация – смешение одной `s`— и одной `p`-орбитали. Две гибридные орбитали расположены на одной оси (прямой) под углом `180^@` друг к другу. Остальные две негибридные орбитали расположены во взаимно перпендикулярных плоскостях. Состояние атома углерода с `sp`—гибридными орбиталями характерно для непредельных углеводородов с тройной связью – алкинов.
В случае, если происходит перекрывание четырёх негибридных атомных орбиталей (по две от каждого атома углерода), то возникает тройная связь. Тройная связь состоит из одной `sigma`- и двух `pi`-связей. `pi`-Связь менее прочная, чем `sigma`-связь, а её электроны легче смещаются в сторону одного из углеродных атомов.
Форму объемной восьмерки имеет орбиталь
Главное квантовое число `n` определяет полную энергию электрона на энергетическом уровне и показывает, из скольких энергетических уровней состоит электронная оболочка атома. Принимает целочисленные положительные значения от `1` до `oo`. В периодической таблице Д. И. Менделеева `n` равно номеру периода.
Орбитальное квантовое число `l` показывает, сколько энергетических подуровней составляют данный уровень и характеризует форму орбиталей. Принимает значения от `0` до `(n – 1)`.
При `n=3`, `l` принимает уже три значения: `0(s)`; `1(p)` и `2(d)`. Таким образом, на третьем уровне три подуровня. Орбитали `d`-подуровня имеют форму двух перекрещенных объёмных восьмёрок либо объёмной восьмёрки с перемычкой (рис. 1).
При `n=4` значений `l` уже четыре, следовательно, и подуровней на четвёртом уровне четыре. К перечисленным выше добавляется `3(f)`. Орбитали `f`-подуровня имеют более сложную, объёмную, форму.
Магнитное квантовое число `ml` определяет число орбиталей на каждом подуровне и характеризует их взаимное расположение.
Принимает значения от `-l` до `+l`, включая `0`.
При `l=1`, `m_l` принимает три значения: `−1`; `0`; `+1`. Значит, орбиталей на данном подуровне (`p`-подуровне) три. Так как `p`-орбитали представляют из себя объёмные восьмёрки (то есть линейной структуры), располагаются они в пространстве по осям координат, перпендикулярно друг другу `(p_x,p_y,p_z)`.
При `l=2`, `m_l` принимает уже пять значений: `−2`; `−1`; `0`; `+1`; `+2`. То есть на `d`-подуровне располагаются пять орбиталей. Это плоскостные структуры, в пространстве занимают пять положений.
Ну и наконец, при `l=3`, то есть на `f`-подуровне, орбиталей становится семь, так как `m_l` принимает семь значений (от `−3` до `+3` через `0`). Орбитали являются более сложными объёмными структурами, и взаимное их расположение ещё более сложно.
`m_s` характеризует собственный момент количества движения электрона и принимает только два значения: `+1//2` и `-1//2`.
Электронная ёмкость подуровня (максимальное количество электронов на подуровне) может быть рассчитана по формуле `2(2l+1)`, а уровня — по формуле `2n^2`.
Всё вышесказанное можно обобщить в Таблице 2.
Таблица 2. Квантовые числа, атомные орбитали и число электронов на подуровнях (для `n
Форму объемной восьмерки имеет орбиталь
Теоретические представления в органической химии
Углерод, его особенности
Тогда как атомы элементов-органогенов имеют обычно степени окисления [кислород (-2), азот (-3), фосфор (+5)], углерод может проявлять в соединениях любые степени окисления от (+4) до (-4). В ходе реакций он может присоединять или отдавать электроны, выступая в роли окислителя или восстановителя. Направление перехода электронов зависит от свойств другого реагента.
Степень окисления есть условный заряд атома, который рассчитывается с учетом того, что общая электронная пара связи между атомами полностью относится к более электроотрицательному атому (электроотрицательность характеризует способность атома удерживать электроны, особенно внешние). Общие пары электронов между атомами одного элемента при определении степени окисления не учитываются.
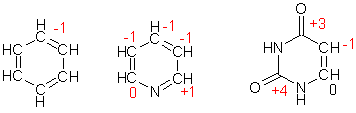
Степени окисления атомов углерода в соединениях
В молекуле органического соединения степени окисления атомов углерода могут быть различными:
Таким образом, степень окисления любого атома углерода в органических соединениях равна алгебраической сумме числа всех его связей с атомами более электроотрицательных элементов (кислород, азот, сера,…), учитываемых со знаком (+), и числа связей с атомами водорода, учитываемых со знаком (-), а все его связи с соседними атомами углерода не учитываются.
Степень окисления является условной величиной, но ее изменение указывает на окислительно-восстановительный характер реакции. Атомы углерода обладают окислительно-восстановительной двойственностью, в органической химии распространены реакции окислительно-восстановительной дисмутации за счет атомов углерода, которые могут протекать как межмолекулярно, так и в рамках одной молекулы.
Гибридные состояния атома углерода.
3. sp-Гибридизация (дигональная), при которой взаимодействуют 1 s и 1 p орбитали. Возникают 2 одинаковых электронных орбитали, расположенные линейно под углом 180°, они имеют форму объемной восьмерки, одна из лопастей которой значительно больше другой. Оставшаяся негибридизованные орбитали взаимно перпендикулярны и перпендикулярны плоскости, в которой лежат sp-гибридные орбитали.