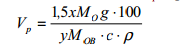Требования к осаждаемой форме. Требования к весовой форме.
Гравиметрические методы анализа. Методы разделения и концентрирования.
Сущность гравиметрического метода анализа. Классификация.
Гравиметрическим анализом называют метод количественного химического анализа, основанный на точном измерении массы определяемого вещества или его составной части, выделенной в элементарном виде, или в виде малорастворимого соединения определенного состава.
Гравиметрические методы делятся на три группы: методы осаждения, методы отгонки и методы выделения. Наиболее распространены методы осаждения, поэтому можно встретить и такую формулировку: гравиметрия – метод количественного анализа, в котором переведенную в раствор составную часть пробы осаждают в виде малорастворимого соединения, по массе которого на основе законов стехиометрии находят количество (массу, массовую долю) определяемого компонента.
Гравиметрические методы разработаны для большинства неорганических анионов и катионов, для нейтральных соединений таких, как вода, диоксид серы, углекислый газ, йод а также для целого ряда органических соединений.
Достоинством гравиметрических методов является их высокая точность: при анализе простых образцов с содержанием определяемого аналита более 1% погрешность анализа можно снизить до 0.1 – 0.2 % что редко удается другими методами. При увеличении сложности состава образца погрешности неизбежно возрастают или приходится затрачивать массу времени на их преодоление.

Требования к осаждаемой форме. Требования к весовой форме.
Осаждаемой формой (ОФ) называют малорастворимое соединение, в виде которого из раствора выделяют определяемый компонент. Часто осаждаемая форма не имеет определенного состава, например, Fe(OH)3·nH2O, Al(OH)3·nH2O. Требования к осаждаемой форме:
2. Осадок должен получаться в форме, удобной для отделения его от раствора (фильтрованием или центрифугированием)и его промывания и не должен быть загрязнен примесями, не удаляемыми при промывке. Как правило, наибольшие проблемы в этом плане представляют аморфные осадки (Fe(OH)3·nН2O, Al(OH)3·nH2O), сильно адсорбирующие посторонние ионы. Кроме того, некоторые кристаллические осадки также сорбируют посторонние ионы (BaSО4) или способны образовывать коллоидные растворы (AgCl). И в том, и в другом случае приходится подбирать особые условия осаждения и промывания осадка, а иногда и маскировать посторонние ионы.
Осадок должен легко и полно переходить в гравиметрическую форму при просушивании или прокаливании. В принципе стараются избегать слишком высоких температур прокаливания (>900–1000°C), но, к сожалению, это не всегда возможно. В подавляющем большинстве случаев высушивание дает менее «точные» результаты, чем прокаливание.
Гравиметрической (весовой) формой (ГФ)называют соединение, массу
которого непосредственно измеряют взвешиванием. Требования к гравиметрической форме:
1. Гравиметрическая форма осадка должна быть стехиометрическим соединением определенного состава. Это абсолютно необходимое условие лежит в основе всех расчетов.
2. Гравиметрическая форма должна иметь высокую химическую устойчивостьна воздухе, то есть не поглощать влагу или CO2, не окисляться кислородом. Так, например, CaO не является идеальной весовой формой, поскольку он весьма гигроскопичен и образует CaCO3 за счет поглощения CO2 из воздуха. В ряде случаев для выполнения этого условия приходится сильно повышать температуру прокаливания: осадок Al(OH)3·nH2O полностью переходит в Al2O3 уже при 700–800°C, но полученный при такой температуре Al2O3слишком гигроскопичен.
3. Желательно, чтобы содержание определяемого элемента в гравиметрической форме было как можно меньше. В этом случае уменьшается погрешность и увеличивается чувствительность анализа.
В ГРАВИМЕТРИЧЕСКОМ МЕТОДЕ АНАЛИЗА



ВЫЧИСЛЕНИЕ РЕЗУЛЬТАТОВ
Ион форма форма
Определяемый осадитель осажденная гравиметрическая
Ион форма форма
Определяемый осадитель осажденная гравиметрическая
ТРЕБОВАНИЯ К НИМ.
ОСАЖДЕННАЯ И ГРАВИМЕТРИЧЕСКАЯ ФОРМЫ.
В гравиметрическом методе осаждения существуют понятия осажденной
Из приведенных примеров видно, что не всегда гравиметрическая форма совпадает с осажденной формой вещества. Различны и требования, предъявляемые к ним.
Осажденная форма должна быть:
· достаточно малорастворимой, чтобы обеспечить практически полное
выделение определяемого вещества из раствора. В случае осаждения
бинарных электролитов ( AgCl; BaS04; СаС2О4 и т. п.) достигается
практически полное осаждение, так как произведение растворимости этих
· полученный осадок должен быть чистым и легко фильтрующимся (что определяет преимущества кристаллических осадков);
· осажденная форма должна легко переходить в гравиметрическую форму.
После фильтрования и промывания осажденной формы ее высушивают или прокаливают до тех пор, пока масса осадка не станет постоянной, что подтверждает полноту превращения осажденной формы в гравиметрическую и указывает на полноту удаления летучих примесей. Осадки, полученные при осаждении определяемого компонента органическим реагентом (диацетилдиоксимом, 8-оксихинолином, α-нитрозо-β-нафтолом и т. д.), обычно высушивают. Осадки неорганических соединений, как правило, прокаливают
Основными требованиями к гравиметрической формеявляются:
· точное соответствие ее состава определенной химической формуле;
· химическая устойчивость в достаточно широком интервале температур, отсутствие гигроскопичности;
· как можно большая молекулярная масса с наименьшим содержанием
в ней определяемого компонента для уменьшения влияния погрешностей
при взвешивании на результат анализа.
Гравиметрический анализ включает два экспериментальных измерения: определение массы навески mнанализируемого вещества и массы продукта известного состава, полученного из этой навески, то есть массы гравиметрической формы mгр.ф анализируемого вещества.
На основании этих данных несложно вычислить массовую процентную долю w, % определяемого компонента в навеске:
Значение гравиметрических факторов, рассчитанное с высокой точностью, приводится в справочной литературе.
Пример 1. Сколько граммов Fе2О3 можно получить из 1,63 г Fе3О4? Рассчитайте гравиметрический фактор.
Р е ш е н и е. Необходимо допустить, что Fе3О4количественно превращается в Fе2О3 и для этого имеется достаточное количество кислорода:
Из каждого моля Fе3О4 получается 3/2 моля Fе2О3. Таким образом, число молей Fе2О3 больше, чем число молей Fе3О4, в 3/2 раза, то есть:
и подставляем в нее численные значения:
m(Fе2О3) = 1,63 ∙(3 ∙ 159,7) / (2 ∙ 231,5) = 1,687 ≈ 1,69 г.
Гравиметрический фактор F равен:

Следовательно, в общем случае гравиметрический фактор определяют по формуле:
F = (а ∙ Мопред.в-во) / (b ∙ Мгр.ф),
Однако не во всех случаях эти расчеты применимы. При косвенном определении железа в Fе2(SО4)3, которое заключается в осаждении и взвешивании BaSО4 (гравиметрическая форма), при расчете аналитического фактора в числителе и знаменателе формулы нет общего элемента. Здесь необходим другой способ выражения химической эквивалентности между этими величинами:
Гравиметрический фактор для массовой процентной доли железа будет выражаться:
Пример 2. Раствор препарата Nа3РО4 ( mн = 0,7030 г) осадили в виде MgNН4РО4∙ 6Н2О. После фильтрования и промывания осадок прокалили при 1000 ˚С. Масса полученного осадка Mg2P2О7 составила 0.4320 г. Рассчитайте массовую процентную долю фосфора в навеске
3.1 Общие положения
3.1.1 Сущность и общая оценка метода. Классификация методов гравиметрического анализа. Общая схема анализа в методе осаждения. Осаждаемая и гравиметрическая формы, требования к ним.
Гравиметрическим анализом называют метод количественного химического анализа, основанный на точном измерении массы определяемого вещества или его составной части, выделенной в элементарном виде, или в виде малорастворимого соединения определенного состава.
Гравиметрические методы делятся на три группы: методы осаждения, методы отгонки и методы выделения. Наиболее распространены методы осаждения, поэтому можно встретить и такую формулировку: гравиметрия – метод количественного анализа, в котором переведенную в раствор составную часть пробы осаждают в виде малорастворимого соединения, по массе которого на основе законов стехиометрии находят количество (массу, массовую долю) определяемого компонента.
Гравиметрические методы разработаны для большинства неорганических анионов и катионов, для нейтральных соединений таких, как вода, диоксид серы, углекислый газ, йод а также для целого ряда органических соединений.
Достоинством гравиметрических методов является их высокая точность: при анализе простых образцов с содержанием определяемого аналита более 1% погрешность анализа можно снизить до 0.1 – 0.2 % что редко удается другими методами. При увеличении сложности состава образца погрешности неизбежно возрастают или приходится затрачивать массу времени на их преодоление.
Недостатками гравиметрических методов являются, во – первых, то, что реагенты, используемые в гравиметрии, за редким исключением, не очень специфичны, поскольку они способны образовывать осадки с группой ионов. Следовательно, требуется предварительное отделение или маскирование мешающих ионов. Во – вторых, как следует из схемы 3.1, в которой представлена последовательность операций гравиметрического анализа в самом общем случае, его длительность и трудоемкость. Поэтому эти методы оправдывают себя, как правило, при анализе единичных образцов, когда требуется высокая точность анализа (см с. ).
Осаждаемой формой (ОФ) называют малорастворимое соединение, в виде которого из раствора выделяют определяемый компонент. Часто осаждаемая форма не имеет определенного состава, например, Fe(OH)3·nH2O, Al(OH)3·nH2O. Требования к осаждаемой форме:
Должна быть обеспечена полнота выделения определяемого компонента (аналита) не менее, чем на 99,9%. Для выполнения этого условия осадок должен обладать очень малой растворимостью: не более, чем
Осажденная и гравиметрическая формы. Требования к ним.
В гравиметрическом методе осаждения существуют понятия осажденной
и гравиметрической форм вещества. Осажденной формой называют соединение, в виде которого определяемый компонент осаждается из раствора. Гравиметрической (весовой) формой называют соединение, которое взвешивают. Иначе ее можно определить как осажденную форму после соответствующей аналитической обработки осадка. Представим схемы гравиметрического определения ионов SO4 2 — , Fe 3+ , Мg 2+
определяемый осадитель осажденная гравиметрическая
определяемый осадитель осажденная гравиметрическая
Из приведенных примеров видно, что не всегда гравиметрическая форма совпадает с осажденной формой вещества. Различны и требования, предъявляемые к ним.
Осажденная форма должна быть:
достаточно малорастворимой, чтобы обеспечить практически полное
выделение определяемого вещества из раствора. В случае осаждения
практически полное осаждение, так как произведение растворимости этих
полученный осадок должен быть чистым и легко фильтрующимся (что определяет преимущества кристаллических осадков);
осажденная форма должна легко переходить в гравиметрическую форму.
После фильтрования и промывания осажденной формы ее высушивают или прокаливают до тех пор, пока масса осадка не станет постоянной, что подтверждает полноту превращения осажденной формы в гравиметрическую и указывает на полноту удаления летучих примесей. Осадки, полученные при осаждении определяемого компонента органическим реагентом (диацетилдиоксимом, 8-оксихинолином, α-нитрозо-β-нафтолом и т. д.), обычно высушивают. Осадки неорганических соединений, как правило, прокаливают
Основными требованиями к гравиметрической форме являются:
точное соответствие ее состава определенной химической формуле;
химическая устойчивость в достаточно широком интервале температур, отсутствие гигроскопичности;
как можно большая молекулярная масса с наименьшим содержанием
в ней определяемого компонента для уменьшения влияния погрешностей
при взвешивании на результат анализа.
Вычисление результатов в гравиметрическом методе анализа
Гравиметрический анализ включает два экспериментальных измерения: определение массы навески mн анализируемого вещества и массы продукта известного состава, полученного из этой навески, то есть массы гравиметрической формы mгр.ф анализируемого вещества.
На основании этих данных несложно вычислить массовую процентную долю w, % определяемого компонента в навеске:
Значение гравиметрических факторов, рассчитанное с высокой точностью, приводится в справочной литературе.
Р е ш е н и е. Необходимо допустить, что Fе3О4 количественно превращается в Fе2О3 и для этого имеется достаточное количество кислорода:
Из каждого моля Fе3О4 получается 3/2 моля Fе2О3. Таким образом, число молей Fе2О3 больше, чем число молей Fе3О4, в 3/2 раза, то есть:
и подставляем в нее численные значения:
Гравиметрический фактор F равен:
Следовательно, в общем случае гравиметрический фактор определяют по формуле:
Однако не во всех случаях эти расчеты применимы. При косвенном определении железа в Fе2(SО4)3, которое заключается в осаждении и взвешивании BaSО4 (гравиметрическая форма), при расчете аналитического фактора в числителе и знаменателе формулы нет общего элемента. Здесь необходим другой способ выражения химической эквивалентности между этими величинами:
Гравиметрический фактор для массовой процентной доли железа будет выражаться:
Пример 2. Раствор препарата Nа3РО4 ( mн = 0,7030 г) осадили в виде MgNН4РО4∙ 6Н2О. После фильтрования и промывания осадок прокалили при 1000 ˚С. Масса полученного осадка Mg2P2О7 составила 0.4320 г. Рассчитайте массовую процентную долю фосфора в навеске
w, %(Р) = 0,4320 ∙ 0,2782 ∙ 100 / 0,7030 = 17,10 %.
Пример 3. При прокаливании загрязненного препарата натрия оксалата mн = 1,3906 г получили остаток массой mгр.ф = 1,1436 г. Определите степень чистоты образца. t
Ре ш е н и е. Следует допустить, что разница между исходной и конечной массами соответствует потере углерода оксида при прокаливании. Анализ основан на измерении этой величины:
2.3 Осаждаемая и гравиметрическая формы.Требования, предъявляемые к ним.
При выполнении весовых определений определяемый компонент смеси, или составную часть (элемент, ион) вещества количественно связывают в такое химическое соединение, в виде которого она может быть выделена и взвешена (так называемая гравиметрическая форма, ранее она именовалась «весовая форма»).
Требования к гравиметрической форме Состав гравиметрической формы после высушивания ( или прокаливания ) должен соответствовать определенной формуле и иметь постоянный состав. Гравиметрическая форма должна быть чистой и не быть гигроскопичной. Гигроскопическую гравиметрическую форму следует взвешивать в тиглях, закрытых крышкой При прочих равных условиях следует выбирать гравиметрическую форму, имеющую большую молярную массу или ту форму, в которой отношение молярной массы гравиметрической формы к молярной массе определяемого компонента будет наибольшим.
Требования к осаждаемой форме.
Основным требованием к осаждаемой форме является достаточно малая ее растворимость. Кроме того, требуется, чтобы структура осадка давала возможность с достаточной скоростью вести фильтрование и отмывание от примесей; необходимо также, чтобы осаждаемая форма достаточно полно превращалась в весовую.
2.4 Выбор осадителя.Расчёт объёма осадителя
Выбор осадителя определяется рядом требований, предъявляемых к осадку. Получающийся осадок ( осаждаемая форма) должен отличаться малой растворимостью в воде, легко отфильтровываться и хорошо отмываться от примесей. Этими свойствами обладают крупнокристаллические осадки. Наконец, осаждаемая форма должна при прокаливании нацело превращаться в весовую форму. Так, осадок Fe ( OH) 3 после прокаливания переходит в Fe203, называемую весовой формой, потому что именно это вещество взвешивают в конце анализа. Весовая форма должна строго соответствовать определенной формуле, по которой производят расчет. Она не должна изменять своей массы на воздухе вследствие поглощения паров или углекислого газа.
Расчет объема раствора реактива-осадителя Vp, производят по формуле:
где 1,5 – коэффициент, показывающий, во сколько раз больше необходимо
взять осадителя; х и у – стехиометрические коэффициенты в уравнении реакции осаждения соответственно для реактива-осадителя и определяемого вещества;
Мo и МOB –молекулярные массы соответственно реактива-осадителя и
определяемого вещества; g – навеска определяемого вещества, г; с – массовая
доля осадителя в растворе, %; ρ – плотность раствора-осадителя, г/см 3